sessile serrated adenoma/polyp (SSA/P) は消化器病理医でなくても馴染みのある疾患概念となってきました。
SSA/Pに細胞異型があるもの (with cytological dysplasia) を見る機会があり、この辺を簡単に学んでいきたいと思います。
・2019
・順天堂大学
・Murakami T, Sakamoto N, Nagahara A
引用先の文献(free access)から
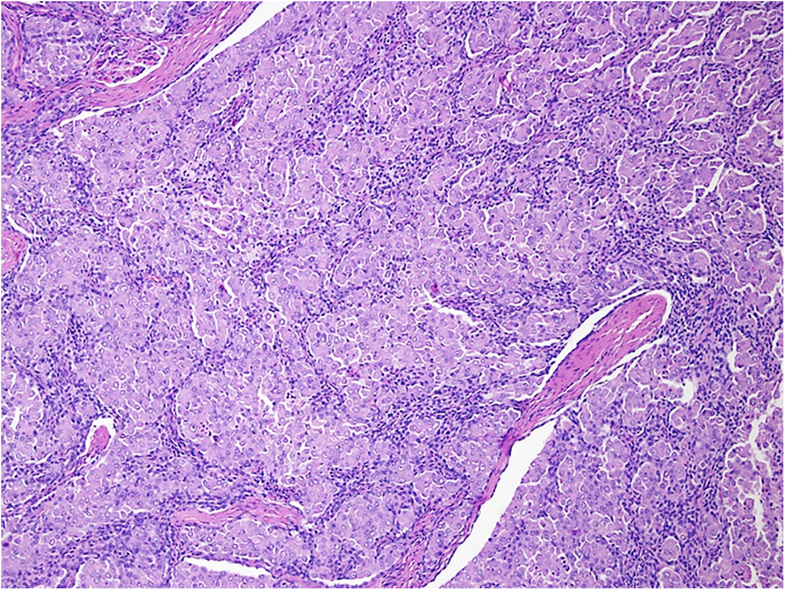
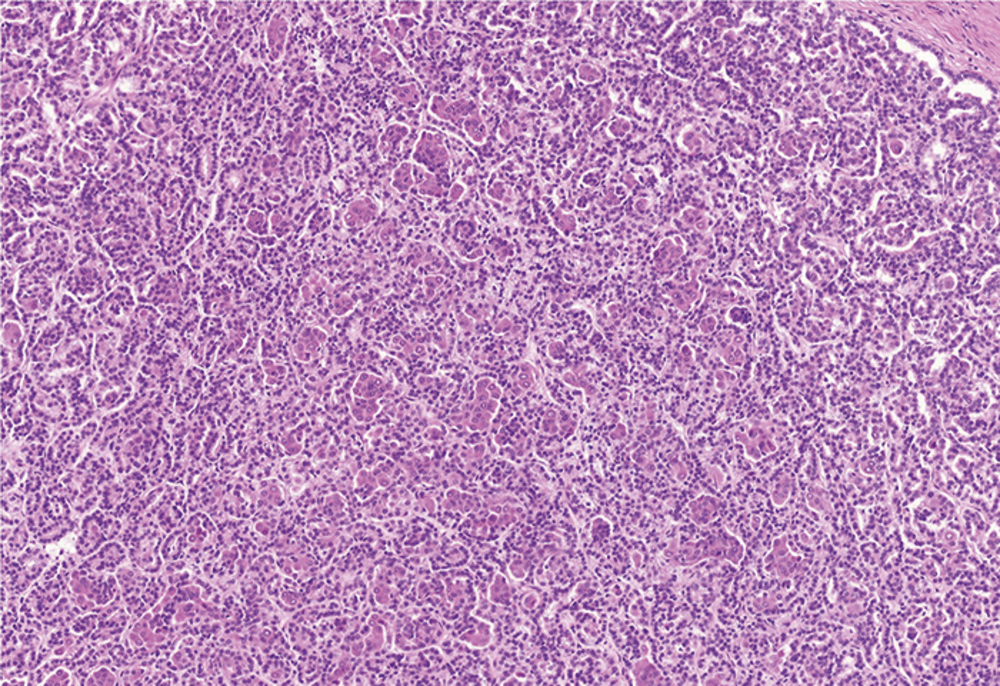
典型的なSSA/Pの組織像として提示されています。
鋸歯状の構築をしめす陰窩には不規則な拡張・不規則な分枝・水平方向への配列 (base)。
いわゆる逆T字・逆L字と呼ばれる形状は特徴的かと。
・SSA/Pは悪性のポテンシャルをもち、serrated neoplasia pathway における早期の前駆病変
・多くはmicrosatellite instability (MSI) の高い大腸癌の発生につながる
・serrated neoplasia pathway は 従来型の adenoma–carcinoma pathway (APC や KRAS の変異)とは異なる経路
SSA/Pの(遺伝子)異常として
・methylation
・loss of protein expression for DNA repair genes such as MLH1
・CpG island methylator phenotype
・BRAF mutations
・lack of genetic alterations in CTNNB1, which is the gene that codes for β‐catenin protein
など
・BRAF‐mutated MSI‐high だけでなく BRAF‐mutated microsatellite stable (MSS) colorectal carcinomas も報告されている
・とくに " BRAF‐mutated MSS colorectal carcinomas " は予後不良
・SSA/Pの中には短期間に浸潤癌になる可能性も示唆されている
・SSA/Pから生じたsm浸潤癌では、リンパ管侵襲やリンパ節転移を生じやすいという報告もある
・頻度は低いものの、SSA/Ps with dysplasia or invasive carcinoma に対するマネジメントは重要
頻度については
・SSA/P with cytological dysplasia は 14%
・SSA/P with invasive carcinoma は 1%
違う報告では
・high-grade dysplasia が 0.2%, sm 浸潤癌が 0.2%
とされている
・この経路での癌化は大腸癌の30%におよぶという報告あり
・一旦癌化してしまえば、癌の進行とともにSSA/Pの成分は消失する
SSA/P with dysplasia or invasive carcinoma に関して
・やや高齢に多い (62 , 65 vs 69才: それぞれwith/without/invasive)
・やや女性に多い (41% vs 59%)
・発生部位は近位の結腸 (proximal colon: proximal to the splenic flexure) が80%以上
という傾向がある。
順天堂大学の研究では, SM浸潤癌(with SSA/P vs with tubular adenoma)に関して
・SM浸潤癌 (with SSA/P) では sessile morphology を示すことが多かった
・SM浸潤癌 (with SSA/P) では よりサイズが小さい
・mucinous component が見られることが多い。
・深く浸潤する傾向は少ない
・が、リンパ管侵襲像は多い
・そして、リンパ節転移も多い (28% vs 7%)
とされています。
内視鏡像やマネジメントなど、さらに詳しくレビューされているので、原文チェックしてみてください。
病理医にとっては内視鏡像になじみがないですが、
内視鏡像と組織像が対比してありましたので原文の画像にリンクしておきます↓
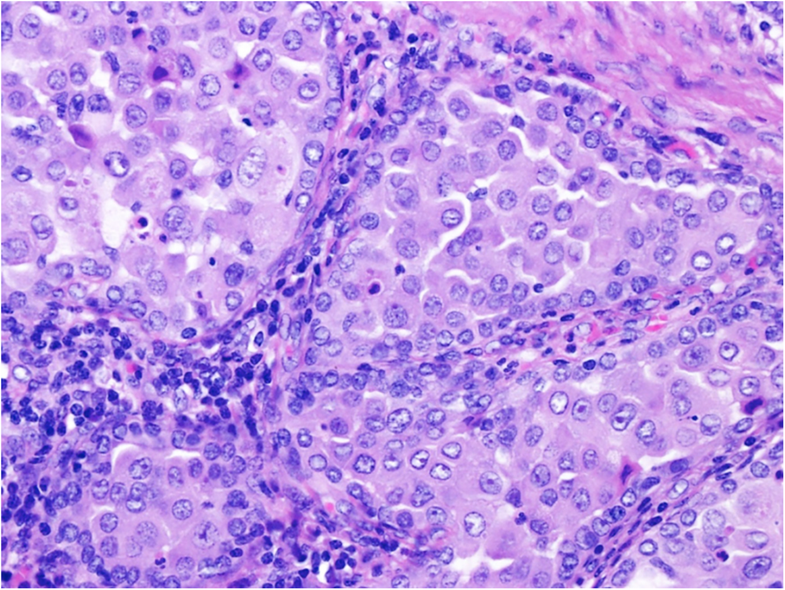
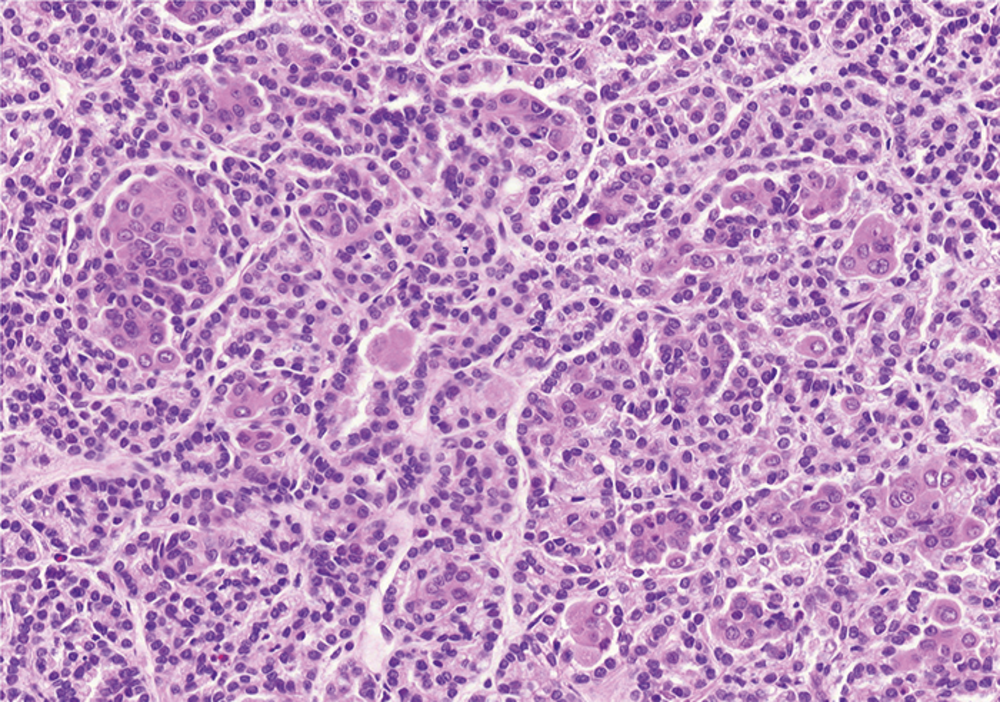
この組織像の右側の部分 (i) が high-grade dysplasia であり、
こういった病変を SSA/P with high-grade cytological dysplasia と呼ぶようです。
結論として、interval cancer (中間期がん)を減らすためにはより注意が必要と書かれています。
病理医としてもSSA/Pについて認識して注意深く診断するように心がけたいと思います。